細胞培養(yǎng)的小腸粘膜有助于了解先天免疫保護免受食物感染。
腸上皮概述了口服攝入的微生物和私人自身間隙環(huán)境之間的界面。 小腸上皮細胞通過跨膜模式識別受體能夠識別微生物配體(1)(2)(3)在防御病原微生物中發(fā)揮關鍵作用。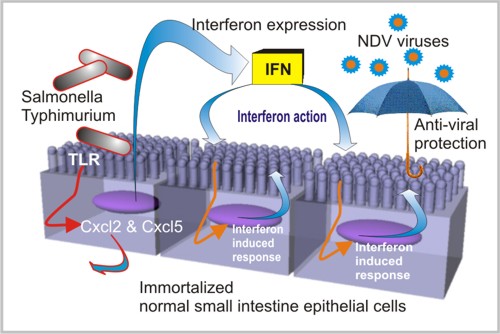

現(xiàn)在,這種非自我認識的功能結果被毫無定義,并且由該保護性鑒定啟動的信號傳導途徑,效應物和調節(jié)機制尚未完全理解。
**近,德GBraunschweig(德G)的Helmholtz感染研究中心的基因調控和分化系的研究小組發(fā)表了一篇文章,介紹了基于小腸成熟細胞的細胞培養(yǎng)的新數(shù)據(jù)(4)。
本文介紹了詳細參考以前的出版物(5)并通過SV40大T抗原(TAg),Krüppel樣因子4(Klf4)的慢病毒轉導永生化的從小鼠E19.5胎兒獲得小腸上皮細胞的有效方法。和DNA結合抑制劑3(Id3)。 在該轉導后約兩個月,細胞顯示出無限增殖的無限增殖性狀,沒有衰老跡象超過一年,長方體形狀,接觸依賴性生長抑制和細胞單層形成。 這些細胞可以通過有限稀釋進行冷凍解凍和亞克隆,表現(xiàn)為顯示腸上皮表型標記的真正永生化細胞系,例如膜結合連接閉塞蛋白(ZO)-1(6),基底外側組織粘附E-鈣粘蛋白(7),間隙連接蛋白連接蛋白43(8),中間絲蛋白波形蛋白,NADPH氧化酶4(Nox4)和三個刷邊界酶,其支持吸收上皮的代謝功能:二肽基肽酶4 ),蔗糖異麥芽糖酶(ISI)和氨基肽酶N(APN),所有這些都已知由腸上皮細胞表達。 重要的是,當這些細胞在反式孔插入物中培養(yǎng)時,它們顯示跨上皮電阻,指示在單層(9)的兩側之間形成緊密屏障的能力(提供腸內內腔和下面的組織)。
使用這種小腸粘膜的體外模型,作者顯示在存在覆蓋上皮細胞單層的介質中稀釋的各種先天免疫配體(Toll樣受體(TLR)4和5配體,脂多糖(LPS)和鞭毛蛋白)所述細胞以表達Cxcl2和Cxcl5的劑量依賴性方式反應。
他們還使用相同的方法來獲得小腸IFN報道子上皮細胞,現(xiàn)在來自轉基因小鼠,旨在研究這些細胞單層對IFN的反應,以增強對病毒感染的保護。 用相同的永生化方案處理的這些細胞類似地作出反應,并提供通過表達螢光素酶作為對INF刺激的細胞反應的報告物響應INF I和III的小腸粘膜的體外模型(IEC-Mx2Luc-10細胞) 10)。為了測試抗病毒保護,使用新城疫病毒(NDV)。 干擾素預處理的單層細胞培養(yǎng)物暴露24小時**80個血細胞凝集單位/ ml NDV。 通過NDV血凝素 - 神經(jīng)氨酸酶(HN)細胞表達的流式細胞術分析對感染水平進行定量,顯示病毒在INF預處理的IECMx2Luc-10細胞中不復制,但在未處理的細胞中確認,證明可以誘導保護性抗病毒條件在用IFN預處理后的IEC-Mx2Luc-10細胞中。 此外,用鼠傷寒沙門氏菌(11)感染的IEC-Mx2Luc-10細胞也能夠產生IFN。 這些實驗與來自細菌感染的IECMx2Luc-10細胞培養(yǎng)物的條件培養(yǎng)基與未感染的IECMx2Luc-10細胞培養(yǎng)物的混合的交叉測試一起顯示了小腸粘膜的這種體外復制物的完全抗病毒保護性質及其用于進一步研究小腸上皮細胞的先天免疫保護作用。






